مقدمة
الأسيتامينوفين، المعروف أيضا باسم الباراسيتامول، هو مسكن وخافض للحرارة يستخدم على نطاق واسع دون وصفة طبية. وبالرغم من أنه آمن بشكل عام عند استخدامه ضمن الجرعات الموصى بها، فإن جرعة زائدة من الأسيتامينوفين هي سبب شائع لفشل الكبد الحاد (ALF)، مما يؤدي إلى مراضة ووفيات كبيرة. ينتج التسمم بالأسيتامينوفين عن كل من الجرعة الزائدة الحادة والتناول المتكرر للدواء فوق الحد العلاجي (RSTI)، والذي يمكن أن يطغى على مسارات التمثيل الغذائي في الجسم ويؤدي إلى تسمم الكبد. تستكشف هذه المقالة علم الأوبئة والفيزيولوجيا المرضية والتشخيص وتدبير التسمم بالأسيتامينوفين.(1)(2)
الامراضيات
يشكل التسمم بالأسيتامينوفين أحد الأسباب الأكثر شيوعاً للتسمم بجرعة زائدة من الأدوية في جميع أنحاء العالم. وهو مسؤول عن عدد كبير من زيارات غرفة الطوارئ المتعلقة بالجرعة الزائدة والاستشفاء كل عام في الولايات المتحدة. يمكن أن يحدث التسمم إما عن قصد (كجزء من محاولة انتحار) أو عن غير قصد بسبب سوء الاستخدام، مثل تجاوز الجرعة اليومية القصوى أو الجمع بين المنتجات المحتوية على عقار الأسيتامينوفين دون الانتباه إلى ذلك. تتضمن الجرعة الزائدة الحادة عادة، جرعة واحدة كبيرة، بينما تنتج السمية المزمنة، أو التناول المتكرر بالجرعات فوق العلاجية RSTI، عن جرعات متكررة تتجاوز 4 جم / يوم لفترة طويلة من الزمن.(3)(2)
الفيزيولوجيا المرضية
يتم امتصاص الأسيتامينوفين بسرعة من الجهاز الهضمي بعد تناوله، ويخضع لعملية التمثيل الغذائي الكبدي على نطاق واسع. في ظل الظروف العادية، يتم استقلاب معظم الدواء إلى كبريتات غير سامة ومركبات الغلوكورونيد المرتبطة، والتي يمت إفرازها في البول. ويتأكسد جزء بسيط بواسطة نظام إنزيم السيتوكروم P450، في الغالب CYP2E1، لتشكيل N-acetyl-p-benzoquinone imine (NAPQI)، وهو وسيط شديد التفاعل. تحت الجرعات العلاجية، يتم إزالة السموم من NAPQI بواسطة الغلوتاثيون الكبدي وتفرز لاحقاً. في حالات الجرعة الزائدة، يتم تجاوز قدرة الغلوتاثيون على إزالة السموم من NAPQI، مما يؤدي إلى تراكم NAPQI، الذي يرتبط بالبروتينات الخلوية، مما يسبب نخر خلايا الكبد وإصابة الكبد.(4)
الأعراض السريرية
تتطور سمية الأسيتامينوفين خلال أربع مراحل متميزة، تتميز كل منها بأعراض محددة ونتائج سريرية تعتمد على الجرعة المبتلعة والوقت منذ تناول الدواء.(4)
مراحل سمية الاسيتامينوفين
المرحلة الأولى: الحضانة (0-24 ساعة)
- الأعراض: قد يكون المرضى بدون أعراض أو يعانون من أعراض غير محددة مثل فقدان الشهية والغثيان والقيء والتعرق.
- النتائج المخبرية: طبيعية بشكل عام؛ ومع ذلك، في حالات الابتلاع الهائل، يمكن ملاحظة العلامات المبكرة لارتفاع إنزيمات الكبد (زيادة مستويات الترانساميناز) أو الحماض اللبني.
المرحلة الثانية: الفترة الكامنة (24-72 ساعة)
- الأعراض: قد تختفي الأعراض الأولية، ولكن يمكن أن يتطور عند المرضى ألم في الربع العلوي الأيمن. وقد يبقى البعض بدون أعراض.
- النتائج المخبرية: إرتفاع في إنزيمات الكبد (AST / ALT) شائعة. قد تبدأ السمية الكلوية في الظهور أيضاً خلال هذه المرحلة.
المرحلة الثالثة: ذروة سمية الكبد (72-96 ساعة)
- الأعراض: تعود الأعراض الجهازية، بما في ذلك الغثيان الشديد والقيء والشعور بالضيق وعلامات الفشل الكبدي مثل اليرقان واعتلال التخثر والاعتلال الدماغي. تحمل هذه المرحلة أعلى مخاطر الوفاة بسبب مضاعفات مثل الوذمة الدماغية أو الصدمة الإنتانية.
- النتائج المخبرية: ذروة ارتفاع الترانساميناسات خلال هذه الفترة؛ خلل وظيفي كبير في الكبد واضح مع ارتفاع مستويات البيليروبين وINR. قد يحدث الفشل الكلوي أيضا.
المرحلة الرابعة: التلاشي (4 أيام إلى 2 أسابيع)
- الأعراض: قد يتعافى المرضى أو يتطور لديهم فشل أعضاء متعددة. يتميز التعافي بالعودة التدريجية إلى وظائف الكبد الطبيعية.
- النتائج المخبرية: تبدأ اختبارات وظائف الكبد في العودة للطبيعي في حالة حدوث التعافي. يشير الارتفاع المستمر لإنزيمات الكبد إلى استمرار الضرر.
الاعتماد على الجرعة
تتأثر شدة السمية بالجرعة المبتلعة:
- تعتبر الجرعات التي تزيد عن 10 غرام أو 200 ملغم / كغم (أيهما أقل) سامة محتملة.
- تصنف الابتلاع الذي يتجاوز 30 غراماً على أنه “ضخم – هائل” ويتطلب استراتيجيات علاج قوية.
التشخيص
يعتبر التشخيص المبكر للتسمم بالأسيتامينوفين أمراً بالغ الأهمية لمنع السمية الكبدية. يستخدم مخطط Rumack-Matthew بشكل شائع لتقييم خطر السمية الكبدية في حالات الجرعة الزائدة الحادة عندما يكون وقت الابتلاع معروفاً. يتم رسم مستويات الأسيتامينوفين في المصل مع مرور الوقت منذ الابتلاع لتحديد ما إذا كان العلاج مبرراً أو لازماً.(5,6)
روماك ماثيو نوموغرام
- يظهر الرسم البياني مستويات الأسيتامينوفين في المصل مقابل الوقت منذ الابتلاع، مما يسمح لمقدمي الرعاية الصحية بتحديد ما إذا كان العلاج باستخدام N-acetylcysteine (NAC) له ما يبرره.
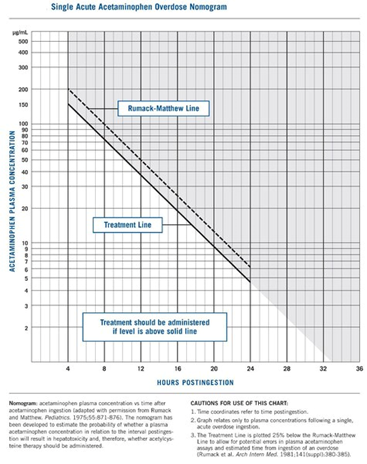
- يشير مستوى الأسيتامينوفين في الدم البالغ 140-150 ميكروغرام / مل بعد 4 ساعات من الابتلاع إلى الحاجة إلى علاج NAC للتخفيف من خطر السمية الكبدية.
- إذا كان وقت الابتلاع غير معروف أو إذا حدث عند المريض تغير في حالته العقلية، فلا يمكن استخدام الرسم البياني بشكل موثوق، ومن الضروري إجراء تقييمات إضافية.
التشخيص في الابتلاع المتكرر فوق العلاجي RSTI أو السمية المزمنة
قد تكون مستويات الأسيتامينوفين في حالات الابتلاع المتكرر فوق العلاجي (RSTI) أو السمية المزمنة، في الدم منخفضة أو غير قابلة للكشف. لذلك، يعتمد التشخيص بشكل أكبر على:(6,7)
- اختبارات وظائف الكبد: تشير المستويات المرتفعة من إنزيمات الكبد مثل AST (الأسبارتات أمينوترانسفيراز) و ALT (ألانين أمينوترانسفيراز) إلى إصابة الكبد.
- دراسات التخثر: تشير النسبة الدولية المنتظمة المرتفعة (INR) إلى ضعف وظائف الكبد.
- قد تشمل الدراسات المختبرية الأخرى لوحة التمثيل الغذائي الكاملة، وتحليل غازات الدم، واختبار مستويات الساليسيلات لاستبعاد ابتلاع سموم أخرى.
المؤشرات السريرية للسمية الكبدية
- مستويات AST وALT المرتفعة، خاصة إذا تجاوزت 1000 وحدة دولية / لتر، توحي بقوة بالسمية الكبدية المرتبطة بالأسيتامينوفين.
- قد ترتفع مستويات البيليروبين الكلّية، مما يشير إلى ركود صفراوي أو خلل في الكبد.
- يمكن أن تحدث الاضطرابات الاستقلابية مثل نقص فوسفات الدم والحماض الأيضي أيضاً نتيجة لإصابة الكبد الشديدة.
التدبير
الدعامة الأساسية لعلاج التسمم بالأسيتامينوفين هي إعطاء N-acetylcysteine (NAC)، وهو ترياق فعال يجدد الغلوتاثيون الكبدي، ويعزز اقتران الكبريتات غير السامة، ويقلل من NAPQI إلى أشكال أقل سمية.
1. الفحم المنشط:
الفحم المنشط هو تدخل مهم في إدارة التسمم بالأسيتامينوفين، خاصة عندما يراجع المريض في غضون أربع ساعات من الابتلاع. يساعد على تقليل امتصاص الأسيتامينوفين من الجهاز الهضمي، وبالتالي التخفيف من آثاره السامة للكبد المحتملة.(8)
إرشادات الإدارة
- التوقيت: يجب إعطاء الفحم المنشط إذا ظهر المريض في غضون 4 ساعات من تناول جرعة سامة محتملة من الأسيتامينوفين.
- الجرعة: الجرعة الموصى بها للبالغين تتراوح بين 50 إلى 100 غرام، بينما بالنسبة للأطفال، تتراوح من 25 إلى 50 غراما.
- موانع الاستعمال: لا ينبغي إعطاء الفحم المنشط إذا كان المريض غير قادر على حماية مجرى الهواء أو إذا كانت هناك موانع أخرى، مثل انثقاب الجهاز الهضمي أو الحالة العقلية المتغيرة بشدة.
الفعالية
- الابتلاع الحاد: لوحظت أكبر فائدة من الفحم المنشط في حالات ابتلاع الأسيتامينوفين الهائل (يعرف عموما بأنه أكثر من 30 غراما).
- التركيبات ذات التحرير طويل الأمد: بالنسبة للتركيبات ذات التحرر طويل الأمد للأسيتامينوفين، قد يظل الفحم المنشط مفيداً حتى بعد فترة الأربع ساعات بسبب خصائص الامتصاص المطولة.
الاعتبارات السريرية
- في المرضى الذين يشتبه في تناول جرعة زائدة حادة، وخاصة أولئك الذين يعانون من ابتلاع عالي الخطورة (أكبر من 200 ملغ / كغ أو 10 غرام)، يمكن أن يلعب الفحم المنشط دوراً حاسماً في تقليل مستويات الأسيتامينوفين القصوى وإصابة الكبد اللاحقة.
- إذا تم إعطاء الفحم المنشط، فإنه لا يمنع الحاجة إلى مزيد من العلاج باستخدام N-acetylcysteine (NAC)، والذي يجب أن يبدأ في أقرب وقت ممكن بناءً على مستويات الأسيتامينوفين في الدم والحُكم السريري.
2. إن-أسيتيل سيستئين (NAC):
N-acetylcysteine (NAC) هو ترياق حاسم للجرعة الزائدة من الأسيتامينوفين، ويمكن أن يتم تناوله عبر طريقين: عن طريق الفم أو الوريد. غالباً ما يعتمد اختيار المسار على السيناريو السريري، وخاصة حالة المريض وتوقيت مراجعة المريض للإسعاف.(9)
طريق التطبيق
NAC عن طريق الوريد
- يفضل في الجرعة الزائدة الحادة: يفضل عادةً NAC عن طريق الوريد لجرعة زائدة من الأسيتامينوفين الحاد بسبب بداية العمل السريعة ومدة العلاج الأقصر.
- بروتوكول الجرعات: يتضمن النظام الوريدي القياسي ما يلي:
- جرعة تحميل 150 ملغ / كغ تسريب على مدى 60 دقيقة.
- تليها جرعة مداومة قدرها 50 ملغ / كغ على مدى 4 ساعات، ثم 100 ملغ / كغ خلال ال 16 ساعة التالية.
- المزايا:
- إدارة أسهل في المرضى الذين قد يعانون من الغثيان أو القيء بشكل كبير.
- تقليل مخاطر أخطاء الجرعات مقارنة بالأنظمة الفموية، والتي تتطلب جرعات أكثر تكراراً.
NAC عن طريق الفم
- الخيار البديل: يمكن استخدام NAC عن طريق الفم عندما يكون الإعطاء عن طريق الوريد غير متاح أو غير عملي.
- بروتوكول الجرعات: يتكون النظام الفموي من:
- جرعة تحميل 140 ملغ / كغ، تليها 70 ملغ / كغ كل 4 ساعات ليصبح المجموع 18 جرعة على مدار 72 ساعة.
- السلبيات:
- يتطلب جرعات أكثر تواتراً، والتي يمكن أن تكون مرهقة.
- ارتفاع معدل حدوث الآثار الجانبية المعدية المعوية مثل الغثيان والقيء.
التوقيت والفعالية
- يكون NAC أكثر فعالية عند تناوله في غضون 8 ساعات من تناول الأسيتامينوفين. يمكن أن تؤدي التأخيرات بعد هذه النافذة إلى زيادة كبيرة في خطر السمية الكبدية.
- في الحالات التي يكون فيها تركيز الأسيتامينوفين في المصل أعلى من خط العلاج في مخطط Rumack-Matthew، يجب بدء NAC على الفور، حتى قبل توفر النتائج المختبرية إذا كان هناك اشتباه قوي في الجرعة الزائدة.
3. زراعة الكبد:
قد يحتاج المرضى الذين لديهم دليل على الفشل الكبدي الخاطف، مثل اعتلال الدماغ واعتلال التخثر، إلى الإحالة إلى مركز زراعة الكبد. تستخدم معايير الكلية الملكية King’s College، والتي تشمل عوامل مثل درجة الحموضة، وINR، ومستويات الكرياتينين، ودرجات اعتلال الدماغ، بشكل شائع لتقييم الحاجة إلى الزرع.
الإنذار
يكون تشخيص سمية الأسيتامينوفين ممتازاً إذا تم إعطاء NAC على الفور، في غضون ثماني ساعات من الابتلاع بشكل مثالي. حتى المرضى الذين يظهر لديهم أعراض في وقت لاحق قد يتعافون مع العلاج المناسب NAC، ولكن خطر الفشل الكبدي والموت يزداد بشكل كبير مع تأخر العرض.(10)
بالنسبة لأولئك الذين يحتاجون إلى زراعة الكبد، تكون معدلات البقاء على قيد الحياة أقل، لا سيما في أولئك الذين يستوفون معايير King’s College. يبلغ معدل البقاء على قيد الحياة بدون زرع من فشل الكبد الحاد الناجم عن الأسيتامينوفين حوالي 70٪، مقارنة بمعدلات أقل بكثير للأسباب الأخرى لفشل الكبد الحاد.
الوقاية
ركزت الجهود المبذولة للحد من جرعة زائدة من الأسيتامينوفين على تثقيف الجمهور والمتخصصين في الرعاية الصحية حول الجرعات الآمنة، والحد من توافر التركيبات عالية الجرعة التي لا تستلزم وصفة طبية، ودمج عبوات آمنة لتقليل مخاطر الجرعة الزائدة غير المقصودة. في المملكة المتحدة، أدت القيود المفروضة على المبيعات التي لا تستلزم وصفة طبية واستخدام عبوات الشرائط إلى انخفاض كبير في حالات الجرعة الزائدة وعدد عمليات زرع الكبد المطلوبة بسبب سمية الأسيتامينوفين.
الاستنتاج
التسمم بالأسيتامينوفين هو السبب الرئيسي لفشل الكبد الحاد، مع نتائج وخيمة محتملة إذا لم يتم علاجه على الفور. يعد التشخيص المبكر باستخدام مخطط Rumack-Matthew، وتطبيق NAC في الوقت المناسب، والرعاية الحرجة المناسبة من المكونات الرئيسية للإدارة. تظل الوقاية من خلال التثقيف العام والتغييرات التنظيمية استراتيجية مهمة للحد من عبء سمية الأسيتامينوفين.
مراجع
1. Fontana RJ. Acute Liver Failure Including Acetaminophen Overdose. Vol. 92, Medical Clinics of North America. 2008.
2. Mehrpour O, Hoyte C, Nakhaee S, Megarbane B, Goss F. Using a decision tree algorithm to distinguish between repeated supra-therapeutic and acute acetaminophen exposures. BMC Med Inform Decis Mak. 2023;23(1).
3. Budnitz DS, Lovegrove MC, Crosby AE. Emergency department visits for overdoses of acetaminophen-containing products. Am J Prev Med. 2011;40(6).
4. Agrawal S, Khazaeni B. Acetaminophen Toxicity [Internet]. StatPearls Publishing; 2023. Available from: https://www.ncbi.nlm.nih.gov/books/NBK441917/
5. Agrawal S, Khazaeni B. Acetaminophen Toxicity [Internet]. StatPearls Publishing; 2023. Available from: https://www.ncbi.nlm.nih.gov/books/NBK441917/
6. Chun LJ, Tong MJ, Busuttil RW, Hiatt JR. Acetaminophen Hepatotoxicity and Acute Liver Failure. 2009.
7. OMALLEY.GERALD. Acetaminophen Poisoning [Internet]. MSD Manuals; 2019. Available from: https://www.msdmanuals.com/professional/injuries-poisoning/poisoning/acetaminophen-poisoning
8. Dart RC, Mullins ME, Matoushek T, Ruha AM, Burns MM, Simone K, et al. Management of Acetaminophen Poisoning in the US and Canada: A Consensus Statement. JAMA Netw Open. 2023;6(8).
9. Smilkstein MJ, Bronstein AC, Linden C, Augenstein WL, Kulig KW, Rumack BH. Acetaminophen overdose: A 48-hour intravenous N-acetylcysteine treatment protocol. Ann Emerg Med. 1991;20(10).
10. Alizadeh N, Yaryari A, Behnoush AH, Raoufinejad K, Behnoush B. Late N ‐acetylcysteine for successful recovery of acetaminophen‐related acute liver failure: A case report . Clin Case Rep. 2023;11(9).




[…] للاطلاع على مناقشة حالات الانسمام بالسيتامول اضغط على الرابط هنا […]